1
/
/
1
帝人ファーマ株式会社
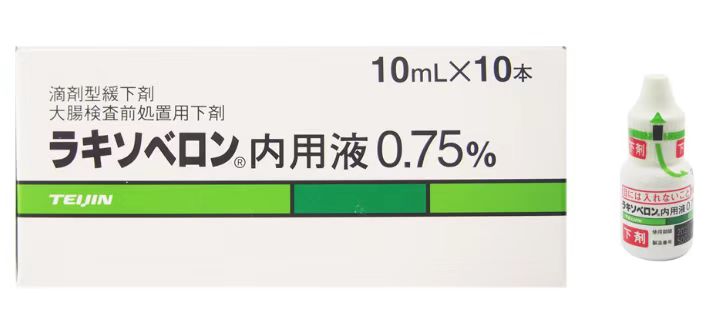
Laxoberon匹可硫酸钠内用液0.75% 10ml×10支 ラキソベロン内用液 0.75% Laxoberon Solution 0.75% 武田 便秘水 比沙可啶钠水合物制剂
Laxoberon匹可硫酸钠内用液0.75% 10ml×10支 ラキソベロン内用液 0.75% Laxoberon Solution 0.75% 武田 便秘水 比沙可啶钠水合物制剂
常规价格
¥5,000 JPY
常规价格
促销价
¥5,000 JPY
单价
/
单价
已含税费。
无法加载取货服务可用情况
匹可硫酸钠内用液通常用于各种便秘、术后辅助排便、注射造影剂(硫酸钡)后促进排便。
一、药品基本信息
- 通用名称:比沙可啶钠水合物制剂(ピコスルファートナトリウム水和物製剤)
- 英文名称:Sodium Picosulfate Hydrate Preparation;Laxoberon Solution 0.75%
- 商品名称:ラキソベロン内用液 0.75%(Laxoberon 内用液 0.75%)
- 剂型:液剂(滴剂型)
-
适应证
- 各种便秘症
- 术后排便辅助
- 造影剂(硫酸钡)给药后的排便促进
- 手术前肠道内容物的排除
- 大肠检查(X 线、内镜)前处置中肠道内容物的排除
-
成分
- 有效成分:日局比沙可啶钠水合物(ピコスルファートナトリウム水和物),含量为 7.5mg/mL
- 添加剤:对羟基苯甲酸甲酯(パラオキシ安息香酸メチル)、氢氧化钠(水酸化ナトリウム)、D - 山梨糖醇(D - ソルビトール)、盐酸(塩酸)
-
性状
- 色調及性状:无色至微黄色的澄明液体,略有粘性,无气味,味甜
- pH 值:5.0~7.5
- 有效成分理化性质:比沙可啶钠水合物为白色结晶性粉末,无气味、无味道;极易溶于水,略溶于甲醇,难溶于乙醇(99.5%),几乎不溶于二乙醚;遇光会逐渐着色。其化学名为 Disodium 4,4’-(pyridin-2-ylmethylene) bis (phenyl sulfate) monohydrate,分子式为C18H13NNa2O8S2⋅H2O,分子量为 499.42
二、用法用量
(一)各种便秘症
- 成人:通常 1 日 1 次,口服 10~15 滴(0.67~1.0mL)
-
小儿:1 日 1 次,按年龄口服,具体剂量如下表,可根据年龄、症状适当增减
| 年龄 | 滴数(mL)|
| ---- | ---- |
|6 个月以下 | 2(0.13)|
|7~12 个月 | 3(0.20)|
|1~3 岁 | 6(0.40)|
|4~6 岁 | 7(0.46)|
|7~15 岁 | 10(0.67)|
(二)术后排便辅助
- 成人:通常 1 日 1 次,口服 10~15 滴(0.67~1.0mL),可根据年龄、症状适当增减
(三)造影剂(硫酸钡)给药后的排便促进
- 成人:通常口服 6~15 滴(0.40~1.0mL),可根据年龄、症状适当增减
(四)手术前肠道内容物的排除
- 成人:通常口服 14 滴(0.93mL),可根据年龄、症状适当增减
(五)大肠检查(X 线、内镜)前处置中肠道内容物的排除
- 成人:通常在检查预定时间的 10~15 小时前,口服 20mL,可根据年龄、症状适当增减
(六)定量滴下型容器使用方法
通常在装有适量水等的容器中,按照图示缓慢挤压瓶身,逐滴滴下
三、禁忌
- 怀疑有急性腹症的患者:肠道蠕动增强可能导致症状恶化
- 对本药成分有过敏史的患者
- 肠道有梗阻或怀疑有梗阻的患者(仅限大肠检查(X 线、内镜)前处置中肠道内容物排除时):肠道蠕动增强可能使梗阻引起的症状恶化,甚至导致肠穿孔
四、注意事项
(一)特殊人群
- 孕妇或可能妊娠的女性:仅在判断治疗益处大于风险时方可给药
- 高龄者:因生理功能通常有所下降,需注意减量等
-
合并症、既往病史患者(仅限大肠检查(X 线、内镜)前处置中肠道内容物排除时)
- 肠道狭窄及重度便秘患者:肠道蠕动增强可能引发缺血性肠炎或肠梗阻,肠梗阻发生时甚至可能导致肠穿孔
- 肠道憩室患者:肠道蠕动增强可能导致病情恶化
(二)用药指导
- 手术前肠道内容物排除时,必要时可联合使用灌肠
- 大肠检查(X 线、内镜)前处置中肠道内容物排除时
- 需确认患者日常排便情况,确保本药给药前 1 日或给药前有正常程度的排便后再给药
- 本药给药后若出现腹痛等异常,需进行腹部检查或影像学检查(单纯 X 线、超声、CT 等),并采取适当措施
- 若患者在家中用药,因出现副作用时可能难以应对,需指导患者避免单独服用
- 需让患者充分摄入水分
- 本药为口服制剂,不可作为眼科用药(点眼)使用
(三)药物保存
- 贮藏方法:室温保存
- 有效期:3 年
五、不良反应
(一)过敏反应
- 皮肤:可能出现荨麻疹、皮疹等(频率不明)
(二)消化系统反应
- 0.1%~5% 未达:腹痛、恶心、呕吐、肠鸣、腹部膨满感、腹泻等
- 频率不明:腹部不适感
(三)其他不良反应
- 肝脏:可能出现 AST 升高、ALT 升高等(频率不明)
- 精神神经系统:可能出现头晕、一过性意识丧失(频率不明),注:大肠检查前处置使用时,可能伴随排便或腹痛引发血管迷走神经反射出现上述症状
- 严重不良反应(仅限大肠检查(X 线、内镜)前处置中肠道内容物排除时)
- 肠梗阻、肠穿孔(频率不明):肠道狭窄患者可能发生肠梗阻,进而可能导致肠穿孔,需充分观察,出现腹痛等异常时及时采取适当措施
- 缺血性肠炎(频率不明):需充分观察,出现异常时及时处理
注:不良反应频率统计包含审批时的临床试验及使用情况调查数据
六、药物相互作用
未提及相关药物相互作用信息
七、药理作用
(一)作用机制(改善代谢异常、调节肠道功能相关)
比沙可啶钠水合物在胃、小肠中几乎不发挥作用,进入大肠后,被大肠菌群来源的酶芳基硫酸酯酶(アリールスルファターゼ)水解,转化为活性型的双酚体(ジフェノール体)。活性型双酚体通过以下作用于肠道黏膜,发挥泻下效果(基于大鼠实验)
- 促进肠道蠕动
- 抑制水分吸收
八、药代动力学
(一)吸收
未明确提及具体吸收程度数据,但提及活性型双酚体部分会被吸收
(二)分布
给大鼠口服14C- 比沙可啶钠水合物 5mg/kg,通过放射性测定及全身 autoradiography 研究发现,药物大部分分布在胃肠道,少量分布于肝脏、肾脏、血液及肺,且反复给药后分布情况几乎无变化
(三)代谢
比沙可啶钠水合物在小肠内不被水解,进入大肠后,被大肠菌群来源的酶芳基硫酸酯酶水解为双酚体;部分双酚体被吸收后,在肝脏中发生葡萄糖醛酸结合反应
(四)排泄
- 大肠中水解生成的双酚体大部分直接随粪便排出
- 部分被吸收的双酚体,经肝脏葡萄糖醛酸结合后, either 随尿液排出,或随胆汁再次分泌到十二指肠,经肠道随粪便排出
- 给大鼠口服14C- 比沙可啶钠水合物 5mg/kg,测定 72 小时内尿和粪便中的排泄量,结果显示给药后 48 小时内几乎完成体内放射性物质排泄;72 小时内,21% 的给药量随尿液排出,72% 随粪便排出
九、临床研究
(一)国内临床试验
在国内共 81 家机构开展临床试验(含双盲试验),对 1679 例疗效判定病例进行统计,各病症有效率如下表
| 病症 | 有效以上(例数 / 总例数) | 有效率 |
|---|---|---|
| 未明确具体病症 1 | 750/899 | 83.4% |
| 未明确具体病症 2 | 57/65 | 87.7% |
| 造影剂排泄促进 | 489/516 | 94.8% |
| 大肠检查前处置 | 154/199 | 77.4% |
十、包装规格
10mL×10(定量滴下型遮光气密容器装)
十一、生产信息
-
生产企业
- 生产销售商:帝人ファーマ株式会社(
- 企业地址:東京都千代田区霞が関3丁目2番1号
Share