1
/
/
1
参天製薬株式会社
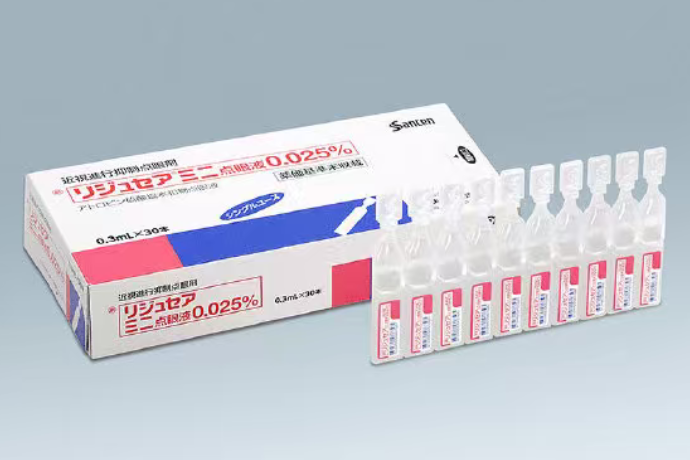
阿托品硫酸盐水合物0.025% 0.3mLx30本 リジュセアミニ点眼液0.025% Atropine Sulfate Hydrate 参天 延缓近视
阿托品硫酸盐水合物0.025% 0.3mLx30本 リジュセアミニ点眼液0.025% Atropine Sulfate Hydrate 参天 延缓近视
常规价格
¥8,000 JPY
常规价格
促销价
¥8,000 JPY
单价
/
单价
无法加载取货服务可用情况
阿托品硫酸盐水合物 0.025% 为抗胆碱滴眼液,通过阻断眼部胆碱受体,发挥散瞳和调节麻痹作用。适用于儿童屈光检查、散瞳验光,及缓解虹膜睫状体炎等眼部炎症。
一、药品基本信息
- 通用名称:阿托品硫酸盐水合物
- 英文名称:Atropine Sulfate Hydrate
- 商品名称:リジュセアミニ点眼液 0.025%、Un 也三二点眼液 0.025%、RYJUSEA Mini ophthalmic solution
- 剂型:滴眼剂
- 适应证:近视进展抑制
- 成分:
- 有效成分:每 1mL 含阿托品硫酸盐水合物 0.25mg
- 添加剂:浓甘油、磷酸二氢钠水合物、柠檬酸钠水合物、羟乙基纤维素、pH 调节剂
- 性状:
- pH:4.0~4.6
- 渗透压比:0.9~1.1
- 性状:无色澄明、无菌水性滴眼剂
二、用法用量
通常,一次 1 滴,一日 1 次,就寝前滴眼。
三、禁忌
- 对本剂成分有过敏史的患者。
- 青光眼及有狭隅角、前房浅等眼压升高诱因的患者(可能引发急性闭角型青光眼发作)。
四、注意事项
- 特殊人群:
- 哺乳期妇女:需综合考虑治疗的益处及母乳营养的益处,权衡是否继续哺乳或中止哺乳。
- 儿童等:未对低出生体重儿、新生儿、乳儿、5 岁以下幼儿开展临床试验。
- 用药指导:
- 点眼后可能因散瞳出现羞明、雾视,症状恢复前应避免使用可能导致坠落的游具、驾驶自行车 / 汽车、操作机械;必要时需佩戴太阳镜,避免直视阳光或强光。
- 使用时,最初的 1~2 滴应丢弃,不可滴眼;点眼时注意容器尖端不要直接接触眼睛;点眼后需睁开眼睑将药液滴入结膜囊内,闭眼并压迫泪囊部 1~5 分钟后再睁眼。
- 与其他滴眼剂联合使用时,需间隔至少 5 分钟以上。
- 本剂不含防腐剂,开封后需一次性使用,剩余药液应废弃。
- 药物保存:
- 室温保存,且需遮光。
- 铝塑包装开封后,应放入附带的遮光用药袋中,在室温下保存,并于 3 个月内使用。
五、不良反应
- 过敏反应:未明确提及。
- 消化系统反应:未明确提及。
- 其他反应:
- 眼部:5% 以上出现羞明;1%~5% 出现视力障碍、雾视、瞳孔障碍;1% 以下出现调节障碍、眼睑湿疹、眼痒。
- 精神神经系统:1%~5% 出现头痛。
六、药物相互作用
与具有抗胆碱作用的药物(如三环类及四环类抗抑郁药、吩噻嗪类药、抗组胺药等)联合使用时,可能增强循环系统、精神神经系统等全身性副作用(因抗胆碱作用相加)。
七、药理作用
- 调整生物膜功能:未明确提及。
- 改善代谢异常:未明确提及。
- 调节血脂:未明确提及。
- 保护血管:未明确提及。
- 其他作用:
- 作用机制:阿托品可能通过视网膜或巩膜的毒蕈碱受体,直接或间接参与巩膜的重塑,从而抑制眼轴伸长。
- 对毒蕈碱受体(M1、M2、M3、M4、M5 亚型)具有非选择性亲和力(体外试验)。
- 近视进展抑制作用:通过对猴玻璃体内给药、对豚鼠、刺鼠及小鼠滴眼,可抑制实验性近视的进展。
八、药代动力学
- 吸收:对 5~15 岁近视患者(10 例)双眼每日 1 次、每次 1 滴,连续滴眼 7 天的研究显示,1 日目血药峰浓度(Cmax)为 19.7±7.0pg/mL,达峰时间(tmax)中位数为 60 分钟(范围 5.0~60 分钟),0~60 分钟药时曲线下面积(AUC0-60min)为 939±370pg・min/mL;7 日目 Cmax 为 16.5±3.6pg/mL,tmax 中位数为 60 分钟(范围 30~60 分钟),AUC0-60min 为 798±188pg・min/mL。
- 排泄:健康成人男性肌内注射 14C - 阿托品 2mg 后,48 小时内 88% 的 14C 经尿液排泄,其中约 50% 为阿托品原形,不足 2% 为托品酸;呼气中未检测到 14C,粪便中仅检测到少量(不足给药量的 0.5%)。
- 分布:对白色豚鼠双眼单次滴入 2%3H - 阿托品溶液后,1 小时眼组织中 3H 浓度最高,浓度从高到低依次为角膜、巩膜、虹膜睫状体、房水、脉络膜、视网膜、玻璃体;对有色豚鼠和白色豚鼠双眼单次滴入 2%3H - 阿托品溶液后,96 小时时有色豚鼠虹膜中 3H 浓度约为白色豚鼠的 8 倍,提示阿托品可能与黑色素结合。
- 代谢:阿托品可经 N - 脱甲基化为去甲阿托品,经氧化反应生成阿托品 - N - 氧化物,经水解反应生成托品和托品酸(基于外国人数据)。
九、临床研究
国内 Ⅱ/Ⅲ 期试验:纳入 5~15 岁、调节麻痹下客观等效球镜度数为 - 1.0D~-6.0D 且 1 年内等效球镜度数进展≥0.5D 的近视患者 299 例,分别给予本剂、0.01% 制剂、普拉洛芬滴眼剂,每日 1 次(就寝前),每次 1 滴,持续 36 个月(治疗 Ⅰ 期 24 个月 + 治疗 Ⅱ 期 12 个月)。结果显示,给药 24 个月后,本剂组与普拉洛芬滴眼剂组相比,调节麻痹下客观等效球镜度数相对于给药前的变化量有统计学显著差异,证实本剂的优越性;给药 36 个月内的变化趋势符合预期。本剂组 122 例中,19 例(15.6%)出现副作用,主要为羞明(9.0%)。
十、包装规格
塑料滴眼容器,0.3mL×30 支(铝塑袋 1 袋含 30 支)。
十一、生产信息
生产企业:参天製薬株式会社
Share